Las mitohondrias se conocieron principalmente como componentes que producen energía celular. Pero los científicos están descubriendo cada vez más que estos pequeños organizaciones funcionan mucho más que solo ANCILL. También se incluyen en funciones inmunes como el control de la inflamación, la regulación de la muerte celular y la respuesta a las infecciones.
Investion de mis colegas y yo descubrimos que las mitocondrias juegan otro papel clave en su respuesta inmune: sentir actividades bacterianas y ayudar a los neutrófilos, el tipo de glóbulos blancos, trampas y matarlos.
En los últimos 16 años, mi investigación se centró en comprender las decisiones de las células inmunes tomando durante la infección y cómo el desglose de estos procesos de toma de decisiones causa enfermedad. El reciente descubrimiento de mi luz de laboratorio es la luz por la cual las personas con enfermedades autoinmunes como el lupus para combatir las infecciones, revelando una potencial conexión entre una mitohondia disfuncional y una defensa inmune debilitada.
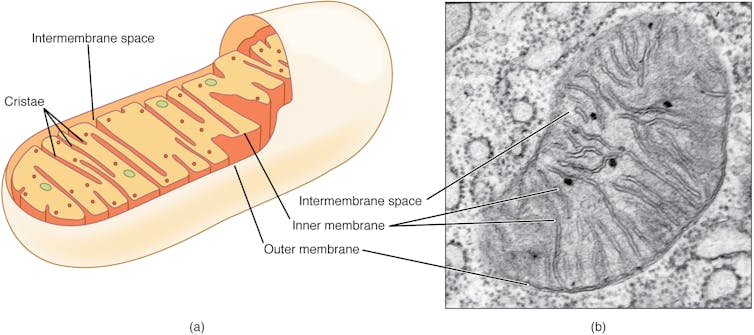
Mitohondria Es mucho más que solo producir energía. OpenStak, CC BI-SA Armas secretas del sistema inmunitario
Los neutrófilos son el tipo más común de células inmunes y sirven como los primeros encuestados del sistema inmune. Uno de sus mecanismos de defensa clave libera trampas o redes neutrofílicas: estructuras más altas compuestas de ADN y proteínas antimicrobianas. Estas redes adhesivas se balancean y neutralizan en los microbios, evitando que se propague en el cuerpo.
Hasta hace poco, los científicos creían que la formación neta se lanzó principalmente con estrés celular y daño. Sin embargo, nuestro estudio ha revelado que las mitohondrias pueden detectar un cierto subproducto bacteriano, lactato) y usar esa señal para iniciar la formación neta.
El lactato generalmente se conecta con fatiga muscular en humanos. Pero en el contexto de las infecciones bacterianas, juega un papel diferente. Muchas bacterias alivian el lactato como parte de su propia producción de energía. Mi equipo descubrió que después de que la bacteria se vio afectada por un compartimento celular llamado Phagon, los neutrófilos pueden sentir la presencia de este lactato.
Dentro del fagosoma, este lactato comunica con neutrófilos que las bacterias están presentes y que los procesos antibacterianos no son suficientes para matar a estos patógenos. Cuando las mitocondrias se encuentran en células neutrofílicas para descubrir este lactato, comienzan a señalar a la célula que resuelva redes que tienen las bacterias nutrientes. Una vez que la bacteria se libera fuera de la célula, otras células inmunes pueden matarlas.
Aquí, neutrófilos envolvió las bacterias MRSA (verde).
Cuando bloqueamos la capacidad de las mitocondrias para sentir lactato, los neutrófilos no pudieron producir red de manera efectiva. Esto significaba que las bacterias tienen más probabilidades de evitar la captura y la proliferación, mostrando cuán crucial es crucial este mecanismo de defensa inmune. Este proceso enfatiza el intrincado diálogo entre el metabolismo de las bacterias y la maquinaria de energía de la energía del huésped.
Lo que esto es sorprendente es que las mitocondrias en las células pueden detectar bacterias atrapadas en fagosomas, aunque los microbios se unen en un área separada. De alguna manera, los sensores mitocondriales pueden recoger señales de estas particiones, una hazaña impresionante de la coordinación celular.
Dirigirse a las mitocondrias para combatir las infecciones
Nuestro estudio es parte de un campo en crecimiento llamado inmunometabolismo, que explora cómo el metabolismo y la función inmune están profundamente entrelazados. En lugar de dar el metabolismo móvil como un medio estricto para generar energía, los investigadores ahora lo reconocen como un impulsor central de las decisiones inmunes.
La mitohondria se sienta en el corazón de esta interacción. Su capacidad para sentir, reaccionar e incluso formar un entorno de células metabólicas les da un papel fundamental para determinar cómo y cuándo se organiza inmune.
Por ejemplo, nuestros hallazgos proporcionan una razón clave por la cual los pacientes con una enfermedad autoinmune crónica llamada lupus sistémica ithematoso a menudo sufren infecciones repetitivas. Las mitocondrias en neutrófilos de pacientes con lupus no sienten correctamente el lactato bacteriano. Como resultado, la producción neta se ha reducido significativamente. Esta disfunción mitoconal podría explicar por qué los pacientes con el lupus son más vulnerables a las infecciones bacterianas, aunque su sistema inmune se activa constantemente debido a la enfermedad.
Esta observación indica el papel central de las mitohondrias en el equilibrio de las respuestas inmunes. Conecta dos problemas aparentemente no relacionados: el certificado inmunitario, como se ve en el lupus y las debilidades inmunes, como la mayor sensibilidad a la infección. Cuando las mitocondrias funcionan correctamente, ayudan a los neutrófilos a establecer un ataque eficiente y dirigido a las bacterias. Pero cuando las mitocondrias están dañadas, este sistema se descompone.
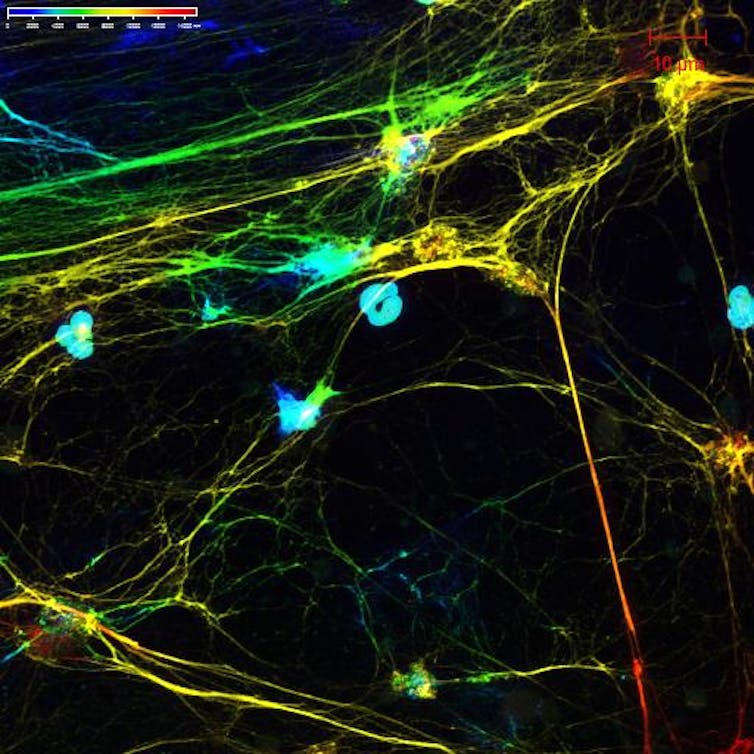
Los neutrófilos que no pueden hacer que los productos de red eficientes contribuyan al desarrollo de lupus. Luz Blanco / Instituto Nacional de Artritis y Enfermedades de Muscin-Bone y Cuero a través de Flickr, CC BI-NC-SA
Nuestro descubrimiento de que las mitocondrias pueden sentir un lactato bacteriano para activar la formación neta abre nuevas oportunidades para tratar las infecciones. Por ejemplo, las drogas que mejoran el sentido mitocondrial podrían aumentar la producción neta en personas con sistemas inmunes alterados. Por el lado, para las condiciones en las que la red contribuye al tejido, como enfermedades graves o autoinmunes, podría ser útil limitar esta respuesta.
Además, nuestro estudio plantea la cuestión de si otras células inmunes usan mecanismos similares para sentir metabolitos microbianos y si otros subproductos bacterianos podrían servir como señales inmunes. Comprender estos caminos podría conducir a nuevos tratamientos que modulan con precisión las respuestas inmunes, reduciendo el daño colateral con la preservación de la defensa antimicrobiana.
Las mitocondrias no son solo el poder celular: estos son los guardias del sistema inmune, advierten incluso las señales metabólicas más importantes de los conquistadores bacterianos. A medida que los investigadores comprenden sus roles se están expandiendo, así como nuestra gratificación de complejidad y adaptabilidad, nuestras defensas celulares.

0 Comentarios